台灣女人連線、立法委員林淑芬辦公室 聯合記者會
妳知道隆乳有淋巴癌的風險嗎?
記者會新聞稿
2019.02.23
今年2月初,15名法國女性因為使用乳房植入物導致健康危害,集體對法國政府和製造商提出刑事訴訟,指控欺騙和危及生命。事實上,法國在去年12月已拒絕展延某廠牌「絨毛型矽膠乳房植入物」的安全許可,因為其與間變性大細胞淋巴癌(ALCL)的關聯。在台灣,此廠牌的絨毛型矽膠乳房植入物經食藥署核准上市,許多女性正在使用此產品。但主管機關卻沒有積極的作為,民眾對此事件毫無所悉,讓女性的健康處於風險之中。
什麼是BIA-ALCL
ALCL是一種罕見的T細胞淋巴癌,可能出現在身體的許多部位。美國FDA在2011年指出有些ALCL的發生和乳房植入物可能有關聯,稱之為BIA-ALCL(Breast Implant-Associated Anaplastic Large Cell Lymphoma),這是屬於免疫系統的癌症,不是乳癌。美FDA日前表示BIA-ALCL病例數量不斷增加,截至2018年9月有457件案例,其中九例已死亡。在有紀錄植入物表面類型的334筆資料中310例為絨毛型,約佔九成。
國際間的作為
- 美國FDA早於2011年便提出BIA-ALCL,針對此病提出風險警訊,並持續蒐集更新相關病例與研究;
- WHO於2016年警示BIA-ALCL是淋巴癌的特有形式,但因為缺乏全球報告與乳房植入物的使用數據,確切的病例數難以掌握;
- 英國成立專家諮詢小組審查乳房植入物相關風險,截至2018年9月有45例確診病例;正在擬訂強制性的醫療植入物登記計劃;
- 澳洲提醒醫護人員,並持續調查國內情形,截至2018年共有72筆病例;
- 加拿大對BIA-ALCL的潛在風險進行審查並持續監控,亦提醒醫護人員,截至2019年1月有22起確診病例;
- 德國已有立法建立國家登記制度的倡議,以改善對乳房植入物等醫療植入物的管控;
- 法國於2016年要求絨毛型植入物的製造廠需提出生物相容性測試;去年12月拒絕展延某品牌絨毛型植入物的安全許可;今年2月召開公聽會,與會專家呼籲禁用此品牌絨毛型植入物,但不贊成已經使用的患者進行預防性手術。
- 歐盟專案小組則認為目前沒有足夠的科學證據來禁止絨毛型植入物的使用。
台灣有沒有BIA-ALCL病例?
根據健保資料,在105年台灣有393人因ALCL就醫,是否跟乳房植入物有關不得而知。因為政府沒有掌握植入物使用的資料,對產品的安全性及有效性也沒有上市後的監測;同時,醫護人員及使用者可能也在沒有警覺的情況下忽略病況,因而沒有通報。
相較各國積極作為,台灣政府僅在2011年及2017年透過公文要醫師進行評估、告知與觀察,並發佈產品安全警訊,但沒有積極地對研議如何對國內使用情形進行調查與瞭解,讓女性健康處於風險之中。
我們認為政府除了被動地等待不良事件通報,需有更積極配套作為。因此呼籲政府:
- 建立全國乳房植入手術登錄制度,以監測植入物與ALCL及其他健康問題的關聯
- 將BIA-ALCL相關說明加入乳房整型/重建手術說明書,提高患者對疾病的理解與警覺
- 加強醫療人員及使用者對BIA-ALCL的認識及保持對疾病的敏感度
附件
說明一
乳房植入物依材質分為鹽水袋和矽膠袋,依其表面狀況分光滑面型和絨毛面型。美國FDA因為安全考量在1992年宣佈禁用矽膠乳房植入物,台灣隨後跟進,一直到2008年才逐步開放果涷矽膠乳房植入物,目前台灣使用的植入物中絨毛型約佔七至八成。而國外BIA-ALCL現有的病例中,大多發生在絨毛型植入物。
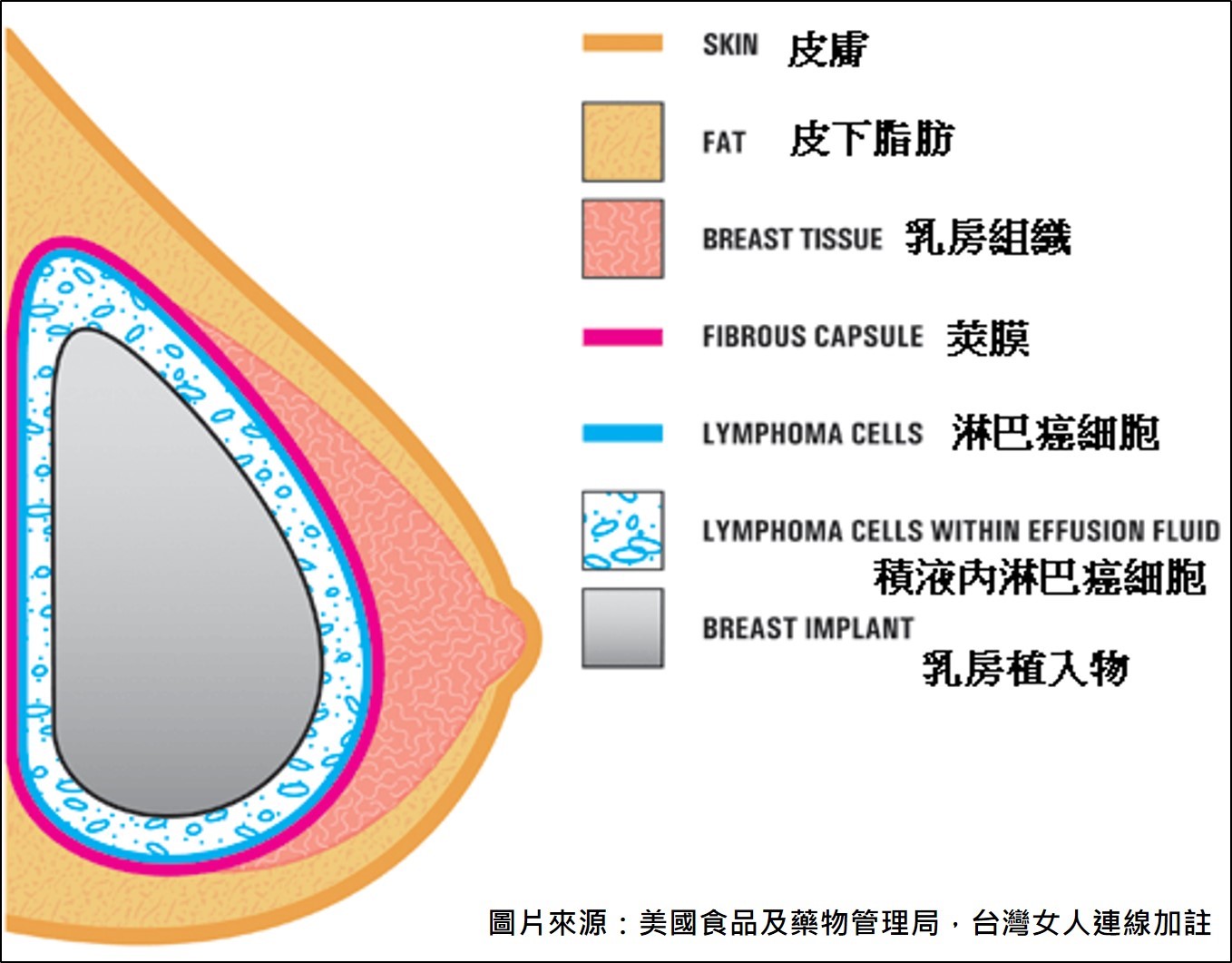
說明二
BIA-ALCL示意圖